Lý thuyết axit nitric và muối nitrat
– Axit nitric HNO3 là một chất lỏng, không màu, bốc khói mạnh ở trong môi trường không khí ẩm có D = 1,53 g/cm3.
– Axit nitric kém bền trong điều kiện thường khi có ánh sáng, dung dịch axit nitric đặc (HNO3đ) khi bị phân hủy một phần sẽ giải phóng ra khí nitơ đioxit (NO2). Khí NO2 tan được trong dung dịch axit, làm cho dung dịch có màu vàng.
– Axit nitric tan nhiều trong nước theo bất cứ tỉ lệ nào. Trong phòng thí nghiệm thường có loại HNO3 đặc, nồng độ 68% có D = 1,40 g/cm3.
Axit HNO3 là một trong các axit mạnh
Axit nitric là một trong các axit mạnh nhất, trong dung dịch loãng có thể phân li hoàn toàn thành ion H+ và ion NO3- .
Dung dịch HNO3 có tính axit nên làm quỳ tím chuyển sang đỏ; có khả năng tác dụng với oxit bazơ, bazơ và muối của axit yếu hơn để tạo ra muối nitrat.
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
Axit HNO3 là chất oxi hóa mạnh
Axit nitric có tính oxi hóa mạnh. Tùy thuộc vào nồng độ của axit và mức độ mạnh yếu của một chất khử mà HNO3 có thể bị khử để tạo ra các sản phẩm khác nhau của nitơ.
Axit nitric có khả năng oxi hóa được hầu hết các kim loại trừ Pt và Au. Khi đó, các kim loại sẽ bị oxi hóa đến mức oxi hóa cao nhất và tạo ra sản phẩm là muối nitrat.
VD: Cu + 4HNO3 đặc → Cu(NO3)2 + 2NO2 + 2H2O
Trong dung dịch HNO3 đặc, nguội, kim loại Al và Fe bị thụ động hóa do 2 kim loại tạo ra một lớp màng oxit bền, bảo vệ cho kim loại khỏi tác dụng của các axit nên, trong thực tế sử dụng bình làm bằng nhôm hoặc sắt để đựng HNO3 đặc.
Khi đun nóng HNO3 đặc, sẽ có thể oxi hóa được một số phi kim như C, S, P,…
VD: 3FeO + 10HNO3 (đ) → 3Fe(NO3)3 + NO + 5H2O
HNO3 đặc còn có khả năng oxi hóa được nhiều hợp chất vô cơ và hữu cơ khác như: vải, giấy, mùn cưa, dầu thông,… dễ bị bị phá hủy hoặc bị bốc cháy khi mà tiếp xúc với HNO3 đặc.
Muối của axit nitric còn có thể được gọi là muối nitrat. Một số muối nitrat như: natri nitrat NaNO3, bạc nitrat AgNO3, đồng(II) nitrat Cu(NO3)2,…
Muối nitrat dễ dàng bị phân hủy trong môi trường nhiệt, giải phóng oxi nên ở nhiệt độ cao thì muối nitrat có tính oxi hóa mạnh.
Muối nitrat của một số các kim loại hoạt động mạnh (K, Na,…) khi bị phân hủy tạo ra muối nitrit và khí O2.
VD: 2KNO3 → 2KNO2 + O2 (nhiệt phân)
Muối nitrat của các kim loại magie, kẽm, sắt, chì, đồng,… khi bị phân hủy tạo sẽ ra oxit của kim loại tương ứng, khí NO2 và O2.
VD: 2Cu(NO3)2 → 2CuO + 4NO2 + O2 (nhiệt phân)
Muối nitrat của các kim loại như: bạc, vàng, thủy ngân,… khi bị phân hủy tạo sẽ tạo ra kim loại tương ứng, khí NO2 và O2.
VD: 2AgNO3 → 2Ag + 2NO2 + O2 (nhiệt phân)
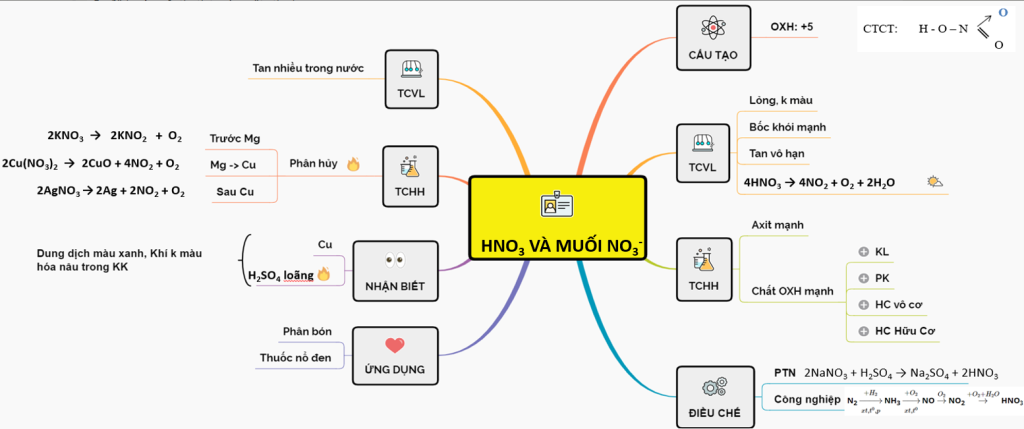
Sơ đồ tư duy bài axit nitric và muối nitrat
Bài tập axit nitric và muối nitrat – Trắc nghiệm axit nitric và muối nitrat
Bài 1: Các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3 đặc, nguội là
Fe, Al, Cr bị thụ động trong HNO3 đặc, nguội.
Bài 2: Khi nhiệt phân, dãy muối nitrat nào đều cho sản phẩm là oxit kim loại, khí nitơ đioxit và khí oxi?
A. Cu(NO3)2, Fe(NO3)2, Pb(NO3)2.
Muối nitrat của các kim loại magie, kẽm, sắt, chì, đồng… bị phân hủy tạo thành oxit kim loại tương ứng, khí NO2 và khí O2.
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2
Tag: 9 violet giảng về 11 giáo soạn