Kali là một nguyên tố hóa học thú vị với nhiều ứng dụng trong đời sống và công nghiệp. Bài viết này sẽ khám phá công thức hóa học của kali, các phương pháp điều chế kim loại này, tính chất vật lý, phản ứng hóa học, và sự tồn tại của nó trong tự nhiên.
Công Thức Hóa Học và Đặc Điểm của Kali
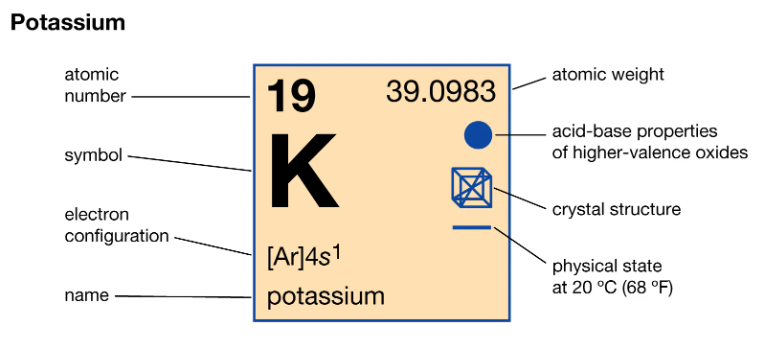
Công Thức Hóa Học của Kali
Kali, ký hiệu hóa học là K, là nguyên tố kim loại kiềm trong bảng tuần hoàn, có số nguyên tử là 19. Kali không tồn tại tự do trong tự nhiên do tính chất cực kỳ hoạt động của nó. Kali thường được tìm thấy dưới dạng hợp chất, như kali clorua (KCl) hoặc kali hidroxit (KOH).
So Sánh với Canxi
So với nguyên tử canxi (Ca), nguyên tử kali có bán kính lớn hơn và ít dày đặc hơn. Điều này là do kali nằm ở chu kỳ 4 của bảng tuần hoàn, trong khi canxi nằm ở chu kỳ 3, làm cho kali có nhiều lớp electron hơn và bán kính nguyên tử được mở rộng.
Phương Pháp Điều Chế Kali
Điều Chế Kali trong Phòng Thí Nghiệm
Kali có thể được điều chế bằng phương pháp điện phân nóng chảy kali hidroxit (KOH) ở nhiệt độ cao. Quá trình này cần điều kiện nhiệt độ và điện áp cụ thể để đảm bảo sự phân ly của ion và hình thành kim loại kali.
Tính Chất Vật Lý Của Kali
Kali là kim loại mềm, có thể cắt được bằng dao. Nhiệt độ nóng chảy của kali là khoảng 63.5 °C, làm cho nó có thể nóng chảy ngay cả khi tiếp xúc với nhiệt độ của cơ thể người.
Phản Ứng Hóa Học của Kali
Phản Ứng với Nước
Kali phản ứng mạnh mẽ và bạo lực khi tiếp xúc với nước, tạo ra kali hidroxit (KOH) và giải phóng khí hiđrô, thường đi kèm với ngọn lửa. Phản ứng này minh họa tính chất hoạt động cao của kali và nguy cơ cao trong việc xử lý.
Phản Ứng với Rượu Etylic
Kali cũng phản ứng với rượu etylic tạo thành kali etoxit, một chất rắn màu trắng, cho thấy khả năng của kali trong các phản ứng hóa học phức tạp.
Tồn Tại Trong Tự Nhiên và Đồng Vị
Kali trong Tự Nhiên
Trong tự nhiên, kali tồn tại chủ yếu dưới dạng ion K⁺ trong các khoáng vật và muối hòa tan. Nó là một phần quan trọng của cân bằng điện giải trong cơ thể sống và có vai trò thiết yếu trong các quá trình sinh học như dẫn truyền thần kinh và co bắp.
Các Đồng Vị của Kali
Kali có hai đồng vị chính tồn tại trong tự nhiên là K-39 và K-40. Trong đó, K-40 là đồng vị phóng xạ và có vai trò trong các nghiên cứu địa chất và xác định tuổi đá.
Kali là một nguyên tố hóa học với nhiều đặc điểm và ứng dụng độc đáo. Hiểu biết về các phản ứng hóa học, phương pháp điều chế và ứng dụng của nó trong công nghiệp và sinh học có thể giúp chúng ta sử dụng kali một cách hiệu quả và an toàn hơn. Kali không chỉ là một phần của bảng tuần hoàn mà còn là một phần không thể thiếu của cuộc sống hàng ngày và các quá trình công nghiệp.